
Источники
- Большая Советская энциклопедия
- Большой энциклопедический словарь
- Большой англо-русский и русско-английский словарь
- Медицинская энциклопедия
- Химическая энциклопедия
- Энциклопедический словарь
- Dictionnaire technique russo-italien
- Естествознание. Энциклопедический словарь
- Большой Энциклопедический словарь
- Источник: Большая советская энциклопедия. — М.: Советская энциклопедия. 1969—1978.
- Источник: Большой Энциклопедический словарь. 2000.
- Источник: Большой англо-русский и русско-английский словарь
- Источник: Медицинская энциклопедия
- Источник: Химическая энциклопедия
- Источник: Энциклопедический словарь
- Источник: Dictionnaire technique russo-italien
- Источник: Естествознание. Энциклопедический словарь
- Источник:
Большая Советская энциклопедия
глиоксалин, 1,3-диазол, бесцветные кристаллы, tкип 256 °С. И. хорошо растворим в воде и спирте, умеренно в эфире. И. ароматичен: легко галогенируется, нитруется, сульфируется и т. д. Водород NH-группы может быть замещен на алкил действием, например, диметилсульфата. И. получают реакцией глиоксаля с аммиаком и формальдегидом. Производные И. широко распространены в животном и растительном мире и имеют важное биологическое значение (Гистамин, Гистидин, Карнозин, Пилокарпин и др.).
Большой энциклопедический словарь
ИМИДАЗОЛ - бесцветные кристаллы, tпл 90 .С. Цикл имидазола - структурный фрагмент многих важных природных соединений, напр., гистидина, пуриновых оснований, витамина В12, а также синтетических лекарственных средств.
Большой англо-русский и русско-английский словарь
imidazole
Медицинская энциклопедия
органическое соединение, представляющее собой пятичленный гетероцикл (1,3-диазол), входящее в состав некоторых аминокислот, алкалоидов, витаминов, ферментов и других физиологически активных веществ; некоторые производные И. используются в качестве лекарственных веществ.
Химическая энциклопедия
(1,3-диазол, глиоксалин), мол. м. 68,08; бесцв. кристаллы с моноклинной решеткой (а= 0,754 нм, b =0,544 нм, с =0,975 нм, b = 117°30'); т. пл. 90 °С, т. кип. 257°С; m 13,28.10-30 Кл. м (диоксан); DH0 обр Ч 60 кДж/молъ (для газа Ч 130 кДж/моль); DH0 возг 67,2 кДж/моль, р К а14,2 (отщепление протона), 7,03-7,25 (присоединение протона).

И. хорошо раств. в воде, этаноле, диоксане, умеренно - в диэтиловом эфире, бензоле, плохо - в углеводородах. Молекулы имеют плоскую конфигурацию и ассоциированы благодаря водородным связям (степень ассоциации более 20). Для И. характерна прототропная таутомерия, вследствие чего положения 4 и 5 равноценны (так, 4- и 5-метилимидазолы идентичны). И. обладает ароматич. св-вами. Атом N-1 обусловливает кислотность И. - способность образовывать соли щелочных и щел.-зем. металлов. По атому N-1 легко образуются также N-алкил-, N-арил-, N-ацилпроизводные и др. Атом N-3 -нуклеоф. центр, по к-рому протекают протонирование, кватернизация и комплексообразование. Наличие атомов N двух типов способствует электроф. замещению в положения 4 и 5, нуклеофильному - в положение 2. Карбоксилирование И. протекает в положения 4 и 5, металлирование N-алкил- и N-аралкилпроизводных - в положение 2. И. устойчив к действию большинства окислителей и восстановителей: не окисляется HNO3, Н 2 СrО 4, КМnО 4, но расщепляется под действием пероксидов; не восстанавливается амальгамой Na, Zn/HCl, HI при 300 °С. N-Ацетилимидазолы в присут. Pd-катализаторов в уксусной к-те гидрируются в тетрагидроимидазолы (имидазолидины), к-рые легко гидролизуются до диаминов. В пром-сти И. и его производные получают взаимод. этилендиамина со спиртами, альдегидами, к-тами или сложными эфирами при 400 °С в присут. Pt/Al2O3, напр..

Лаб. методы синтеза: взаимод. a-дикетонов с формальдегидом и NH3 в ледяной СН 3 СООН; конденсация глиоксаля с NH3 и СН 2 О; декарбоксилирование 4,5-имидазолдикарбоновой к-ты. И. - структурный фрагмент молекул пурина, гистамина, гистидина, пилокарпина, уреидов, трансферинов, витамина В 12 и др. Производные И. - лек. препараты (дибазол, прискол, нирванол и др.). Дикето- и трикетоимидазолидины, такие, как гидантоины, парабановая к-та, аллантоин и др., -антисептики и инсектициды. Лит.: Пожарский А. Ф. [и др.], "Успехи химии", 1966, т. 35, в. 2, с. 261 -92; Гарновский А. Д. [и др.], "Успехи химии", 1973, т. 42, в. 2, с. 177-205; Общая органическая химия, пер. с англ., т. 8, М., 1985, с. 429-88; Grimraett М. R., в кн.: Advances in heterocyclic chemistry, v. 12, N.Y., 1970, p. 103-83. А. Д. Гарновский.
трuс -ИМИДАЗОЛИДОФОСФАТ, соед. ф-лы I, мол. м. 248,15; бесцв. кристаллы; т. пл. 135-137°С; раств. в ТГФ, диоксане, нитрометане; водой гидролизуется. В спектре ЯМР 31 Р хим. сдвиг d 16,3 м. д. В ряду полных амидов Н 3 РО 4 отличается повыш. реакц. способностью по отношению к нуклеофилам НХ, где X = OR, SR, NHR, NR2, RC(O)O и др. Р-ции протекают с замещением имидазольных групп; при избытке НХ и повыш. т-ре м. б. достигнуто полное их замещение.

Получают И. р-цией РОСl3 с имидазолом в среде ТГФ, а также взаимод. РОСl3 с соед. ф-лы II. И. используют в биохимии для фосфорилирования соед., содержащих группу ОН. В тех же целях чаще используют более реакционноспособный mpuc -триазолидофосфат (получают действием 1,2,4-триазола на РОСl3 в среде диоксана в присут. триэтиламина). Лит.:Houben Weyl, Methoden der organischen Chemie, 4 Aufl, Bd. 12, Tl. 2, Stuttg., 1978, S. 465-472. Г. И. Дрозд.
Энциклопедический словарь
имидазо́л
бесцветные кристаллы, tпл 90ºC. Цикл имидазола — структурный фрагмент многих важных природных соединений, например гистидина, пуриновых оснований, витамина В12, а также синтетических лекарственных средств.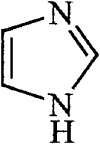
* * *
ИМИДАЗОЛИМИДАЗО́Л, бесцветные кристаллы, tпл 90 °С. Цикл имидазола — структурный фрагмент многих важных природных соединений, напр., гистидина(см. ГИСТИДИН), пуриновых оснований, витамина В12, а также синтетических лекарственных средств.
Dictionnaire technique russo-italien
м.
imidazolo m, iminazolo m
Естествознание. Энциклопедический словарь
гетероциклич. соединение, бесцв. кристаллы, tnл 90 0С. Цикл И. - структурный фрагмент мн. важных природных соединений, напр. гистидина, пуриновых оснований, витамина B12, а также синтетич. лекарств. средств.